Už je to tu: jarné alergie
Prinášame Vám peľový kalendár na jarné mesiace.
Môžete si stiahnuť vo formáte pdf TU
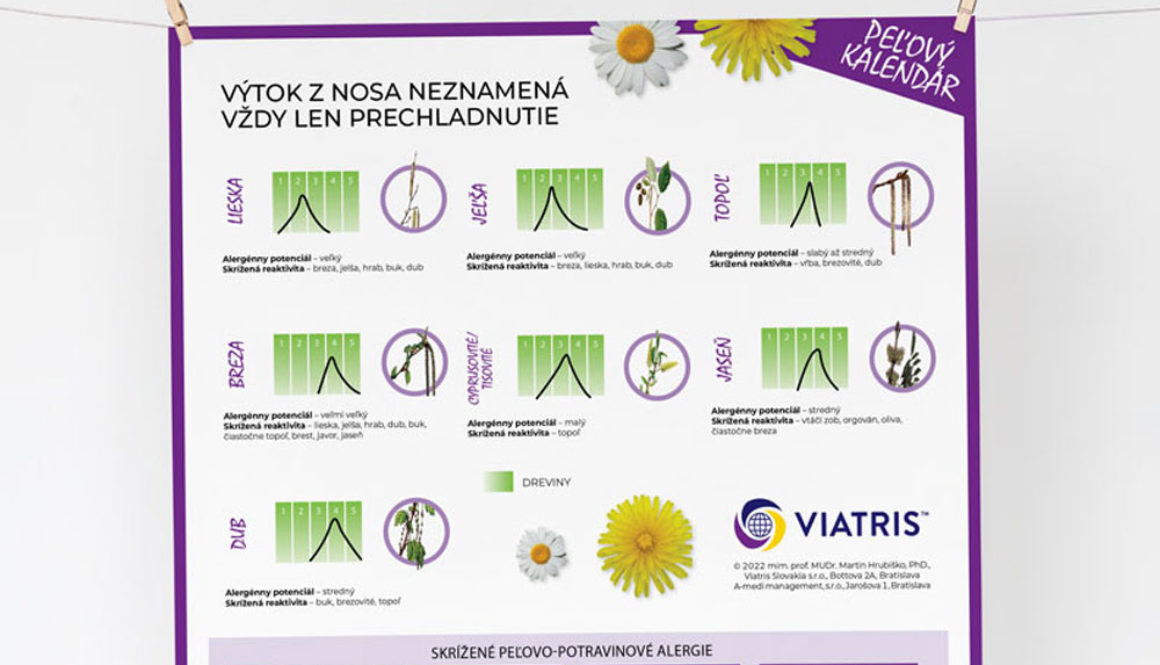
Prinášame Vám peľový kalendár na jarné mesiace.
Môžete si stiahnuť vo formáte pdf TU

Nechcem napísať, že za domáce čipsy, len slovo „domáce“ v mnohých evokuje, že je niečo zdravšie a pritom to tak vôbec nemusí byť. Minimum, čo ale doma pečené koláče a slanosti vedia zabezpečiť je to, že to nie sú ultra spracované priemyselné výrobky – pokiaľ tieto nepoužijeme v rámci surovín.
Ako napríklad, keď použijeme droždie – ktoré je priemyselný výrobok…
Ale poďme naspať ku krekrom, ktoré si viete pripraviť aj bezlepkovo.
Ako mierku som použila kávovú šálku na lungo a z tohto množstva som upiekla 7 plechov krekrov. Znie to „veľa“, ale verte, že je to dávka tak na jeden večer k dobrému filmu 🙂
1 šálka ľanových semiačok
1 šálka maku (mletý alebo celý, je to jedno)
1 šálka slnečnicových semiačok
1 šálka tekvicových semiačok
1 šálka sezamových semiačok – kľudne rôznej farby)
3 – 4 šálky múky
2 šálky studenej vody
1 šálka oleja (najlepší je hroznový alebo repkový olej, pokiaľ je možné nerafinovaný)
1 PL soli
Všetky suroviny premiešame a necháme odstáť, aby semienka nasiakli vodu. Môžeme pridať trocha vody podľa potreby tak, aby cesto malo konzistenciu ako halušky.
Vezmeme dva papiere na pečenie (alebo jeden väčší kus preložíme ako hárok papiera). Dáme 1 veľkú lyžicu cesta na stred papiera, prikryjeme druhým papierom a vyvaľkáme ho na tenko ako papier. Tým, že cesto je olejové, vrchný papier na pečenie hravo stiahneme z cesta.
Naznačíme štvorčeky – aké veľké krekre chceme mať (alebo pásiky, trojuholníky) – použijeme silikónový krájač alebo príborový nožík.
Takto pripravené cesto dáme piecť do vyhriatej rúry na 180 stupňov na 10 – 14 minút. Záleží od toho, ako vám pečie rúra, sledujte si to.
Po upečení krekre rozlámeme podľa toho, ako sme si ich naznačili a necháme vychladnúť.
Skúsime nechať vychladnúť 🙂
Dobrú chuť.

(vegan, bezlakto, bezlepko, bez cukru)
Nielen koláč je dokonalý vtedy, keď je nadýchaný. Aj hummus. Viete ako to dosiahneme?
Základom klasického hummusu je cícer. Zvoliť si môžeme:
Suchý cícer treba najprv namočiť na min. 12 hodín podobne ako ostatné strukoviny. Až potom ho varíme. Ale možno ste doteraz pripravovali hummus z cíceru zo skla, či z konzervy tak, že ste ho už neprevarili. Aj ja som to tak robievala. Nikdy mi môj hummus nechutil tak fantasticky, ako napríklad v arabskej reštaurácii. Ale potom som spravila túto zmenu a odvtedy je môj hummus tá TOPka.
Začala som variť aj hummu z konzervy a zo skla. Odporúčam vyskúšať nasledovne. K hummusu budeme potrebovať ešte:
Postup:
Ak chcete cícer dochutiť, môžete na to použiť napríklad:
Cícer je bohatým zdrojom bielkovín a vlákniny a mali by sme ho zaradiť do jedálnička na pravidelnej báze. Ochutnali ste už „rezne“ z cícera? Voľačo fantastické. Napíšeme nabudúce.
Prípravu hummusu si môžete pozrieť aj vo forme nášho videa na FB a IG Týždeň prevencie.

Diabetológovia, ale hlavne internisti a kardiológovia, venovali v poslednej dekáde pri liečbe diabetikov 2. typu viac pozornosti hlavne úprave tradičných kardiovaskulárnych (KV) rizikových faktorov než dokonalej úprave glykémií – iste hlavne preto, že väčšina používaných antidiabetík (s výnimkou metformínu) nedokázala doteraz ovplyvniť morbiditu a mortalitu týchto chorých.
V oblasti výberu antidiabetika pre rizikového diabetika sa kládla hlavná pozornosť na to, aby liečivo „neškodilo” chorému, a preto sa napr. tiazolidín-dióny nedávali chorým, alebo sa ich užívanie u chorých zastavilo. Uprednostnila sa teda bezpečnosť liečby „hyperglykémie”.
Úprava glykémií v dlhodobom režime sa obvykle ponechávala diabetológovi, príp. endokrinológovi.
Dve regulačné liekové telesá rozhodli, že každé ďalšie nové antidiabetikum musí v klinickej štúdii preukázať svoju KV bezpečnosť (hlavne z hľadiska KV mortality, ale i z hľadiska výskytu vážnych KV príhod) a úpravu dysglykémie.
Tieto telesá od výrobcov ešte vyžadovali, aby v týchto štúdiách boli zaraďovaní KV rizikoví diabetici:
a tiež vyžadovali, aby štúdie dlhšie trvali, a tak ponúkli aj longitudinálne údaje o KV bezpečnosti antidiabetika.
Významným prekvapením tohto prístupu k vývoju nových antidiabetík bola však skutočnosť, že niektoré nové randomizované klinické štúdie nielenže dokladovali KV bezpečnosť (niektorých) nových antidiabetík, ale aj ich KV „protektívnu účinnosť” – osobitne s významnou redukciou KV, ale i celkovej mortality.
Za zmienku iste stojí i tá skutočnosť, že v týchto (práve spomínaných) štúdiách boli zaradení práve „typickí diabetici” s KV ochoreniami a problémami. Ale tieto skvelé výsledky, hlavne u KV chorých diabetikov, ponúkajú aj cestu k úprave liečebného prístupu k dnešnému typickému (KV chorému či KV rizikovému) diabetikovi 2. typu. Hlavne preto, že takto liečený diabetik významne profituje z liečby – má lepšiu (KV) prognózu. A to je obrovské poznanie posledných rokov.
Diabetici majú vyšší výskyt KV ochorení, nakoľko hyperglykémia podporuje:
Ale v posledných asi 2 dekádach významne poklesol v Európe (aj u nás) výskyt infarktov myokardu i cievnych mozgových príhod – vysvetľuje sa to lepšou liečbou antihypertenzívami (užívanou hlavne kombinovanou liečbou) i statínmi (podávame vyššie dávky, a užívame častejšie silnejšie statíny) a platí to i u diabetikov.
Čo sa „prebojovalo” na čelo výskytu KV ochorení u diabetikov je dnes hlavne srdcové zlyhávanie. Ďalej sa preukázalo, že ak sa u diabetika vyvinie KV ochorenie, tak ohromne stúpa jeho (predčasná?) mortalita.
Asi od kardiológa nebudeme očakávať riešenie „hyperglykémie”.
Kardiológ má pomôcť včasnejšie rozpoznať prítomnosť KV ochorenia u diabetika – a ono vzniká pomerne rýchlo a často nenápadne (asymptomaticky).
Druhou úlohou kardiológa je rozpoznať (včasne) prítomnosť diabetu 2. typu u osoby prezentujúcej sa kardiologickým ochorením (infarktom myokardu, mozgovou príhodou, SZ a pod.) – aj toto je dnes veľmi časté v klinickej prax.
Nuž treba siahnuť hlavne po antidiabetikách, ktoré preukázali v klinických štúdiách aj zlepšenie prognózy KV ochorenia (jeho morbiditu aj mortalitu).
Diabetológ obvykle asistoval pri dôkaze, že pacient má diabetes (napr. indikáciou oGTT) a u diabetika riešil nielen problém hyperglykémie, ale i kontrolu pridružených ďalších KV rizikových faktorov:
Ak je však diabetik i KV chorý, tak aj od diabetológa očakávame „zmenu” prístupu k farmakoterapii hyperglykémie s využitím nových liečiv s prídavným (ale veľkým) KV benefitom.
S novými antidiabetikami prebiehajú i ďalšie klinické štúdie.
Sú medzi nimi aj štúdie u diabetikov bez KV ochorenia – ktoré nám našepkajú, či vieme zabrániť (oddialiť) vzniku KV ochorenia u diabetikov. Tieto štúdie musia byť počtom chorých väčšie a musia i dlhšie trvať – nakoľko pacienti (diabetici) sú tu KV zdraví.
Výsledky a klinickú aplikáciu možno očakávať asi do 5 rokov.
Nuž oblasť „kardio-diabetu” je dnes zaujímavá, živá – a možno z jej rozvoja očakávať zlepšenie KV prognózy našich diabetikov.
Zdroj: Kardiol. Prax 2017, Prof. MUDr. Ján Murín, CSc
Slovensko patrí spolu s krajinami strednej a východnej Európy medzi regióny s vysokým rizikom tzv. odvrátiteľných ochorení. Mnohé z nich, resp. riziko ich vzniku vplyvom spôsobu životného štýlu, sú výrazne bagatelizované ľuďmi.
Vysoká konzumácia ultraspracovaných potravín, pričastá konzumácia mäsových výrobkov, mäsa, sladkostí, sladených nápojov, alkoholu a naopak, nízka konzumácia zeleniny, strukovín a čistej vody – je slovenská norma.
Slovenská diabetologická spoločnosť zorganizovala v minulosti v rámci Národného diabetologického programu Ministerstva zdravotníctva SR projekt „Prevalencia diabetes mellitus na Slovensku“. Primárnym cieľom projektu bolo síce zistiť reálny počet diabetikov v dospelom veku, ale jeho súčasťou bolo aj mapovanie výskytu jednotlivých komponentov MS a ďalších rizikových faktorov ICHS na Slovensku. V rámci projektu bolo celkovo vyšetrených 1625 respondentov, z ktorých sa zhodnotilo 1517 v rámci kompletného súboru údajov, váženého podľa veku, pohlavia a krajov. Náhodne vybraní respondenti boli odosielaní na ďalšie vyšetrenie do 40 diabetologických centier, zriadených vo všetkých 8 krajoch a pokrývajúcich tým celé územie Slovenska.
U respondentov sa v určených diabetologických centrách vykonali objektívne klinické vyšetrenia, zahŕňajúce:
Odobrala sa 1 skúmavka s 5 ml venóznej krvi so stabilizátorom (fluorid) na vyšetrene glykémie a lipidogramu a odoslala kuriérnou službou do referenčného laboratória v Národnom endokrinologickom a diabetologickom ústave v Ľubochni.
U respondentov sa štandardne vyšetrovala:
Respondenti, ktorí nemali doteraz potvrdený DM a ich glykémia nalačno dosiahla hodnoty 5,6 – 6,9 mmol/l, t.j. mali pozitívne kritérium pre HGN, boli pozvaní na vyšetrenie orálneho glukózového testu (oGTT).
Na porovnanie sa použili aj kritériá Medzinárodnej diabetologickej federácie (IDF) pre európsku populáciu:
Prevalencia MS na Slovensku podľa kritérií bola 20,1 %, pričom bola významne vyššia u žien 23,9 % oproti mužom 15,9 %. Výskyt MS sa zvyšoval s nárastom BMI.
Prevalencia hyperglykémie podľa kritérií (nad 6,1 mmol/l) bola v našej populácii 10,4 %, bez štatisticky významnému rozdielu medzi mužmi 10,3 % a ženami 10,6 %. Jej výskyt sa progresívne zvyšoval s vekom.
Prevalencia hyperglykémie bola významne vyššia v skupine s centrálnou obezitou 17,3 %, s celkovou nadhmotnosťou s BMI 27-29 kg/m2 15,4 % a obezitou s BMI nad 30 kg/m2 16,3 %.
Celková prevalencia DM na Slovensku bola 7,0 %, pričom v 5,3 % išlo o známy DM, 1,2 % o novozistený DM podľa ADA kritérií a 0,5 % o novozistený DM po vykonaní oGTT u respondentov s HGN. Prevalencia známeho a novozisteného DM podľa ADA kritérií bola iba nevýznamne vyššia u žien 7,2 % oproti mužom 5,9 %, progresívne sa zvyšovala s vekom. Výskyt DM bol významne vyšší u jedincov s celkovou 12,5 % a centrálnou 12,3 % obezitou.
Centrálna obezita podľa kritérií sa u nás vyskytovala u 29,7 % jedincov a bola významne vyššia u žien 36,9 % oproti mužom 22,0 %. Je to ovplyvnené pravdepodobne rozdielnymi kritériami obvodu pásu pre obe pohlavia.
Prevalencia celkovej obezity s BMI nad 30 kg/m2 (20,4 %) sa v závislosti od pohlavia nelíšila a bola 20,6 % u mužov a 20,3 % u žien. V našej populácii parametre celkovej a centrálnej obezity úzko korelujú a jedinci s celkovou obezitou s BMI nad 30 kg/m2 majú zároveň centrálnu obezitu v 81 % (75 % mužov, 87 % žien) podľa kritérií a 93 % (92 % mužov, 94 % žien). Prevalencia centrálnej obezity sa zvyšovala s vekom a vyskytovala sa až u 55 % jedincov starších ako 60 rokov.
Prevalencia hypertriacylglycerolémie (HTG) nad 1,7 mmol/l u nás bola 25,4 % a bola významne vyššia u mužov (30,1 %) ako u žien (21,2 %). Progresívne sa zvyšovala s vekom, ale na rozdiel od iných komponentov MS výskyt HTG bol najnižší v skupine mužov so základným v porovnaní s vysokoškolským a stredoškolským vzdelaním. Podobne ženy so základným a stredoškolským vzdelaním mali oproti vysokoškolsky vzdelaným ženám nižšiu prevalenciu HTG.
Prevalencia HTG bola vyššia u jedincov s centrálnou obezitou (36,4 %) a v rovnakej miere u jedincov s nadhmotnosťou (36 %) a celkovou obezitou (34 %) v porovnaní s chudými jedincami s BMI pod 25 kg/m2 (14 %). Jej výskyt bol vyšší u chorých s DM (41 %) a HGN (48 %) v porovnaní s jedincami s normálnou homeostázou glukózy (20 %).
Prevalencia nízkych hladín HDL podľa kritérií u nás bola prekvapivo veľmi vysoká – až 55,7 % (44,6 % mužov, 65,9 % žien).
Závislosť prevalencie nízkeho HDL od iných rizikových faktorov bola u oboch pohlaví rozdielna, pričom u mužov sa viac vyskytoval v skupine fajčiarov a paradoxne menej v skupine s HTG a HT.
U žien výskyt súvisel s celkovou a centrálnou obezitou, ako aj s prítomnosťou hyperglykémie podľa kritérií a celkovou prevalenciou DM a podobne ako u týchto komponentov MS bol najvyšší v skupine so základným vzdelaním.
Prevalencia HT (TK nad 140/90) u nás bola 33,0 %, bez významných rozdielov medzi mužmi (33,9 %) a ženami (32,1 %).
Prevalencia zvýšených hodnôt TK podľa kritérií (nad 130/85) bola 43,8 % s významne vyšším výskytom u mužov (48,2 %) oproti ženám (39,9 %) a progresívnym nárastom v závislosti od veku až na hodnoty 74 % vo vekovej skupine nad 60 rokov.
U oboch pohlaví prevalencia zvýšených hodnôt TK, ako aj HT bola významne vyššia pri obezite, pričom jedinci s celkovou obezitou mali v 60 % HT a 72 % zvýšené hodnoty TK a s centrálnou obezitou podľa kritérií v 58 % HT a 70 % zvýšené hodnoty TK.
Celková prevalencia MS (20 %) na Slovensku, ako krajine s vysokým výskytom ICHS, je porovnateľná s prevalenciou v európskej populácii v krajinách so stredným a nízkym rizikom jej výskytu.
Prevalencia jednotlivých komponentov MS však má v rámci európskej populácie svoje špecifiká.
Zdroj: Interná medicína 2007, Peter Galajda, Marián Mokáň, Dana Prídavková, Viera Tomášková, Ľudovít Šutarík, Ľudmila Kručinská, Andrea Bukovská, Gabriela Rusnáková

Chrípka počas tehotenstva prebieha oproti bežnej populácii častejšie s komplikáciami a býva spojená aj s hospitalizáciou. Očkovanie poskytuje ochranu matiek.
Chrípka je respiračné ochorenie, ktoré sa prenáša z človeka na človeka.
Šíri sa čiastočkami aerosólu, ktorý obsahuje vírusy chrípky, z chorého na zdravého jedinca. Vysušený vírus môže prežiť pri izbovej teplote aj niekoľko dní.
Vylučovanie vírusu chrípky u nakazeného sa začína deň pred prvými klinickými príznakmi a pretrváva 5-7 dní.
Inkubačný čas je 12 – 72 hodín.
Chrípka má na Slovensku sezónny charakter s maximom výskytu v zimných mesiacoch, ale vyskytnúť sa môže počas celého roka. Typickým príznakom chrípky je jej náhly začiatok.
Osoba sa cíti:
Sezónna chrípka postihuje predovšetkým najmladšie a najstaršie vekové skupiny, osoby s chronickými ochoreniami:
Rizikovou skupinou sú aj tehotné ženy.
Protilátky, ktoré neutralizujú vírus chrípky, predstavujú dôležitý obranný systém človeka. Po prekonaní infekcie je jedinec chránený pred novou infekciou rovnakým vírusovým kmeňom niekoľko rokov, avšak vírus neustále mutuje.
Po zaočkovaní sa vytvoria protilátky proti vírusom obsiahnutým vo vakcíne.
Preto by sa očkovanie proti chrípke malo vykonávať každý rok pred nástupom chrípkovej sezóny.
Očkovanie proti chrípke má zásadný význam pre osoby s vysokým rizikom vrátane tehotných žien. Asi dva týždne po očkovaní 70 – 90% osôb dosiahne protektívnu hladinu protilátok.
Na Slovensku sa zistilo, že SARI (syndróm akútnej respiračnej insuficiencie) sa u tehotných žien vyskytoval štatisticky významne častejšie ako v ostatnej populácii SR a že úmrtia na SARI u tehotných žien boli štatisticky významne častejšie ako úmrtia na SARI v ostatnej populácii SR.
Ochorelo 13 žien a 6 z nich zomrelo.
Najmladšia tehotná žena so SARI, ktorá zomrela, mala 17 rokov.
Najstaršia tehotná žena so SARI mala 36 rokov.
Vo viacerých prácach bol deklarovaný negatívny dosah chrípky na priebeh tehotenstva.
Niektoré fyziologické zmeny v tehotenstve vedú k vyššiemu riziku ťažšieho priebehu a s tým súvisiacich komplikácií chrípky pre tehotnú (zvlášť v druhom a treťom trimestri) a na plod vrátane:
Fyziologické zmeny počas tehotenstva sa najviac dotýkajú imunitného systému a fyzikálnych pomerov vo vnútorných orgánoch.
Tehotné ženy sú citlivejšie na niektoré intracelulárne parazity vrátane vírusových. Fyzikálne pomery v oblasti panvy, v hrudnej a brušnej dutine sú spojené so zvýšenými nárokmi na kardiovaskulárny a respiračný systém.
Priamy vertikálny prenos vírusu z matky na plod je raritný. Mechanizmus, ktorým dochádza v priebehu chrípky k poškodeniu plodu, je pravdepodobne spojený s horúčkou. Horúčka matky v prvom trimestri je vo zvýšenej miere spájaná s rázštepmi neurálnej trubice a inými vrodenými abnormalitami. Chrípka počas tehotenstva je spájaná so 4-násobne vyšším výskytom fetálnych neoplázií (lymfatický a hemopoetický systém, neoplázia je nádor, nový útvar), aj keď ich absolútny počet je nízky.
Odporúčania sú založené na 4 základných postulátoch:
Očkovanie chráni pred ochorením, hlavne pred jeho ťažkými formami vyžadujúcimi hospitalizáciu a tiež pred úmrtím ženy počas tehotenstva, ale aj v popôrodnom období. Redukuje potrebu antivirotík a tiež riziko vzniku rôznych sekundárnych bakteriálnych komplikácií, čo je dôležité zvlášť v krajinách s vysokou rezistenciou na antibiotiká.
Plod je chránený materskými protilátkami počas tehotenstva a ich prenosom cez placentu aj v prvých mesiacoch života dojčaťa. Benefitom je, že zaočkovaná matka nenakazí svoje dojča po celé obdobie chrípkovej sezóny.
Očkuje sa každý rok sezónnou vakcínou do ramena intramuskulárne, na severnej pologuli sa očkovanie začína v októbri.
Tehotné ženy sa očkujú bez ohľadu na dĺžku gravidity, aj v prvom trimestri. Súhrnné charakteristiky lieku pri všetkých troch u nás najviac používaných inaktivovaných vakcínach uvádzajú, že sa môžu používať vo všetkých štádiách gravidity. Najväčšie množstvo údajov o bezpečnosti je dostupných z podávania počas druhého a tretieho trimestra. Údaje z používania vakcíny proti chrípke na celom svete však nenaznačujú, že by vakcína mohla mať nežiaduci vplyv na plod alebo matku.
Prospešnosť očkovania tehotných pre matku a plod inaktivovanou vakcínou bola dávno dokázaná pri eliminácii novorodeneckého tetanu. Túto skúsenosť môžeme v súčasnosti použiť na ochranu matiek a detí aj pomocou iných inaktivovaných vakcín ako napr. proti čiernemu kašľu, pneumokokovým invazívnym nákazám či chrípke.
Zdroj: Gynekologická prax, doc. MUDr. Mária Štefkovičová, PhD

Všeobecne sa udáva, že človek rozumný – Homo sapiens sa začal objavovať na Zemi asi pred 200 000 rokmi, pritom jeho predchodcovia sa tu vyvíjali asi posledný milión rokov.
Ak si však uvedomíme, že prvé živé organizmy, teda baktérie, vírusy…, sú na Zemi už viac ako 3 miliardy rokov, je zrejmé, že Homo sapiens „prišiel“ už do sveta kolonizovaného pestrým spektrom mikroorganizmov, a tak sa musel nejako vyrovnať s ich prítomnosťou.
Zo systematického pohľadu sa tak vyvinuli 3 formy vzájomnej interakcie a existencie:
Táto mutuálna symbióza ma veľký význam po celý život makroorganizmu a jej zloženie a postupná kolonizácia významne ovplyvňujú mnohé ľudské funkcie, najmä tráviace, imunologické, ba aj mentálne funkcie.
Kolonizácia mikroorganizmami a vznik jednotlivých ník mikrobiómu človeka sa začína už počas vnútromaternicového života, avšak najvýznamnejšia je kolonizácia počas pôrodu a v prvých 2 rokoch života. Celé toto obdobie zahŕňa približne 1 000 dní a v tomto čase máme aj najviac možností vhodne (ale aj nevhodne) zasiahnuť do tohto fyziologického procesu mikrobiálnej kolonizácie s jej želanými či neželanými následkami.
Najvýznamnejšou nikou mikrobioty je tá, ktorá je asociovaná s gastrointestinálnym traktom (GALT) a je vlastne najväčším imunologickým orgánom cicavcov. V tomto dynamickom systéme môžeme nájsť stovky druhov mikroorganizmov, ktoré majú špecifické funkcie, majú početné vzájomné interakcie, ale aj interakcie s receptormi sliznice tráviaceho traktu, a zároveň žijú v zložitej a krehkej rovnováhe. Túto skupinu mutualisticky pôsobiacich mikroorganizmov nazývame súhrnne probiotiká – telu prospešné baktérie.
vedú k vzniku dysbiózy (dysmikróbie).
Následky tejto dysbiózy môžu byť rôzne a môžu sa niekedy prejaviť skoro po ich vzniku alebo s odstupom času a môžu sa prejaviť aj na viacerých orgánoch vrátane imunitného, napr. vo forme alergií. Nedostatočná stimulácia imunitného systému nepatogénnymi mikroorganizmami v ranom živote je podstatou aj tzv. hygienickej teórie zvýšeného výskytu alergií a autoimunitných ochorení v súčasnosti.
Pre správny priebeh kolonizácie organizmu, najmä tráviaceho traktu, a tiež pre udržanie potrebnej krehkej fyziologickej rovnováhy je potrebná aj podpora „priateľskej“ probiotickej mikroflóry, a to najmä látkami, ktoré preferenčne probiotické baktérie metabolizujú:
Z toho vyplýva aj význam samotnej výživy dojčaťa a batoľaťa, a to už od narodenia.
Ideálnou potravou v prvých 4 – 6 mesiacoch jeho života je materské mlieko vlastnej matky, avšak s potrebou zavádzania vhodných prídavkov už v období tzv. imunologického okna, ktoré sa otvára asi v 4. – 6. mesiaci života.
Z uvedeného zase logicky vyplýva, že práve prvé 2 roky postnatálneho života sú z pediatrického hľadiska obdobím, keď možno u dieťaťa významne – pozitívne, ale aj negatívne – ovplyvniť napr. výskyt alergií.
V súčasnosti má už veda poznatky o špecifických pozitívnych účinkoch niektorých konkrétnych kmeňov probiotík, taktiež o pozitívnych efektoch niektorých konkrétnych oligosacharidov, ba aj o biologických efektoch špecifických synbiotík. Synbiotiká sú zmes prebiotík, ktoré selektívne stimuluje rast určitého probiotického kmeňa.
Tieto poznatky sa začínajú uplatňovať aj v praxi a je k dispozícii napr. vo forme hypoalergénnej formuly s obsahom synbiotika. Aktívne tak už dnes máme, vo forme funkčnej potraviny, možnosť využívať jednu z foriem prevencie alergických ochorení u detí.
Je to v našich rukách.
Zdroj: Pediatria 2019, doc. MUDr. Milan Kuchta, CSc.

Celiakia a diabetes mellitus 1. typu patria medzi choroby s autoimunitnou patogenézou a obe sa môžu vyskytovať spoločne u jedného pacienta ako tzv. asociované ochorenia.
Celiakia s diabetes mellitus 1. typu (DM1) patrí k najčastejšie sa vyskytujúcim pridruženým, autoimunitne podmieneným chorobám hneď po tyreopatiách.
Vzájomný vzťah medzi cukrovkou 1. typu a celiakiou je známy vyše 40 rokov.
V odbornej literatúre sa po prvýkrát v roku 1962 opísali konkrétne prípady diabetikov 1. typu s príznakmi celiakie. Postupne sa zistilo, že spoločný výskyt diabetes mellitus 1. typu a celiakie nie je vôbec náhodný.
V európskej populácii sa vyskytuje 10-krát častejšie ako v ostatnej populácii.
Rozdielny výskyt v jednotlivých krajinách je pravdepodobne následkom:
Navyše sa ukazuje, že výskyt celiakie pri diabete 1. typu stúpa s dĺžkou trvania cukrovky.
Súčasný výskyt celiakie a DM 1. typu svedčí o ich spoločných genetických a imunogenetických aspektoch. Predpokladá sa, že ide o rovnaký patogenetický mechanizmus poškodenia tkanív.
Celiakia sa zriedka vyskytuje pred diagnózou diabetu. Vo väčšine prípadov je celiakia diagnostikovaná až po kratšom alebo dlhšom období od manifestácie cukrovky.
Často však celiakia prebieha ako „tichá“ forma.
Dôležitý je preto dlhodobý opakovaný skríning s vyšetrovaním protilátok proti gliadínu, endomýziu a najmä proti tkaninovej transglutamináze, najmä u všetkých detí s DM 1. typ, s frekvenciou raz ročne.
U pacientov s potvrdenou celiakiou je nevyhnutné zavedenie bezlepkovej diéty. Kombinácia diabetickej a bezlepkovej diéty v praktickom živote je často veľmi problematická a ťažká.
Liečba oboch asociovaných ochorení spočíva na 2 pilieroch.
Diéta je striktne bezlepková a navyše treba regulovať obsah a zloženie sacharidov. Vytvoriť špeciálnu diétu pre pacientov s celiakiou a diabetom môže byť problematické. Na zostavenie diabetickej bezlepkovej stravy je zväčša potrebná spolupráca pacienta s odborníkom na výživu (nutricionistom), ktorý má prax v zostavovaní oboch diét.
Úlohu zohráva aj ľudský faktor, pretože zabezpečiť dodržiavanie bezlepkovej diéty pacientmi s diabetom je zložitejšie ako v prípade ľudí, ktorí majú celiakiu „iba“ ako samostatné ochorenie. Súvisí to aj so spoluprácou pacienta, ktorý sa musí vyrovnať s dvoma chronickými ochoreniami, ktoré si vyžadujú špeciálnu dietetickú starostlivosť.
Z praktických skúseností vyplýva, že s dodržiavaním diétnych opatrení to majú ľahšie tí, ktorí majú lepšiu motiváciu. Sú to chorí s klinickými prejavmi celiakie. Spolupráca pacientov s ľahkými alebo žiadnymi symptómami je zložitejšia, tí zväčša bezlepkovú diétu nedodržiavajú.
Väčšina autorov uvádza, že 30-40 % pacientov s DM a celiakiou bezlepkovú diétu nedodržiava.
Po začatí bezlepkovej diéty sa vyrovnajú koncentrácie glykémií počas dňa a zlepší sa metabolická kompenzácia, čím poklesne i neskorší výskyt mikrovaskulárnych a neurologických komplikácií. Liečbou celiakie sa pozitívne ovplyvňuje aj výskyt redších, hnačkovitých až vodnatých stolíc, ktoré sa väčšinou dávajú do súvisu s diabetom. Ak mal pacient tráviace ťažkosti, zlepšia sa obyčajne už po 2 až 3 týždňoch od začatia dodržiavania bezlepkovej diéty. Zlepšenie metabolickej kontroly diabetu po začatí bezlepkovej diéty však nenastáva bezprostredne, ale v priemere až po šiestich mesiacoch.
Zdroj: MUDr. Magdaléna Pašková, časopis Pediatria 4/2009

Vzťah medzi infekciou Helicobacterom pylori (HP) a refluxovou chorobou pažeráka (GERD) nie je do súčasnosti jednoznačne vysvetlený a vedú sa polemiky, či infekcia HP má ochranný, neutrálny alebo indukujúci účinok na GERD.
Kľúčové slová: infekcia Helicobacter pylori, GERD, epidemiológia, patofyziológia, gastritída, ezofagitída, reflux
Epidemiologické štúdie GERD sú založené väčšinou na klasických klinických príznakoch:
Diagnóza infekcie HP je väčšinou založená na vyšetrení bioptickej vzorky žalúdka (histológia, ureáza, kultivácia/citlivosť) alebo na antigénovom teste stolice, respektíve sérologickom vyšetrení krvi.
Prevalencia HP je v Európe rôznorodá, najnižšia je vo Švajčiarsku: 18,9 % a najvyššia v Portugalsku: 86,4 %. Po roku 2000 celkovo v Európe klesla zo 48,8 % na 39,8 %. V Severnej Amerike klesla ešte výraznejšie a to zo 42,7 % na 26,6 % a v Austrálii z 26,6 % na 18,7 %. Naopak, v krajinách Ázie prevalencia HP mierne vzrástla, a to z 53,6 % na 54,3 %. V Južnej Amerike mierne klesla z 62,8 % na 60,2 %.
Vzhľadom na nejednotnosť názorov na vplyv Helicobactera pylori a jeho eradikácie na GERD je vysvetlenie patofyziologických mechanizmov relatívne zložité. Fyziologický reflux, ktorý je asymptomatický, hrá dôležitú úlohu v očiste pažeráka. HP neprežíva v normálnej ani zápalovo zmenenej sliznici pažeráka, keďže tam za štandardných okolností nie je prítomný typ žalúdočného epitelu. Logickým dôsledkom bolo uvažovanie o ovplyvnení sekrécií žalúdočných štiav infekciou HP, čo môže mať vplyv na GERD. Zistilo sa, že zmena sekrécie žalúdočnej šťavy závisí od rozsahu a miesta postihnutia infekciou HP. Prítomnosť potravy v žalúdku stimuluje žalúdočnú sekréciu a rozsah stimulácie sekrécie HCl závisí od zloženia a množstva potravy.
U pacientov s infekciou HP sa sekrécia HCl líši v závislosti od veku, rozsahu zápalového postihnutia a atrofie. Infekcia HP v detstve sa v priebehu rokov až desaťročí postupne rozšíri z antra na telo žalúdka, čo vedie k progresii atrofie a postupnému úbytku parietálnych buniek. Pri antrálnej/pylorickej HP gastritíde prítomná zvýšená produkcia interleukínu-8 (IL-8) stimuluje antrálne G-bunky, čo vedie k hypergastrinémii a následnej hypersekrécii HCl. Pri postihnutí korporálnej sliznice zohráva dôležitejšiu úlohu TNF-alfa a IL-1beta, ktorý inhibuje sekréciu HCl 100x silnejšie ako PPI(16). Čiže rozvojom korporálnej gastritídy dôjde k rýchlemu úbytku sekrečnej schopnosti HCl a riziko GERD klesá, zatiaľ čo riziko rozvoja karcinómu žalúdka stúpa. U pacientov s antrálnou gastritídou s hypersekréciou HCL eradikácia HP infekcie znižuje stimuláciu tvorby kyseliny znížením tvorby IL-8.
Rozdiel v prevalencii medzi európskymi a ázijskými populáciami je daný rozdielmi v životospráve, genetickými faktormi, ale aj virulenciou lokálnych kmeňov HP.
Kmene HP s vysokou virulenciou (faktory oipA, dupA, CagA, VacA s1m1) indukujú masívny zápal korporálnej žalúdočnej sliznice s hypochlórhydriou, rizikom až závažnej atrofie, vredu a karcinómu žalúdka. Bolo dokázané, že väčšina východoázijských HP kmeňov sú CagA a VacA s1m1 pozitívne kmene s vysokou virulenciou. Toto je dôvod rozdielnych posteradikačných rizík GERD, a to vo významne vyššej incidencii GERD vo východázijských populáciách oproti európskym: 21 % k 9 %(17). Rovnako bol v ázijských štúdiách zaznamenaný výrazne vyšší nárast incidencie GERD po úspešnej eradikácii infekcie HP oproti neúspešným pokusom (RR: 4,53, 95 % CI: 1,66 – 12,36)(18). V iránskej štúdii bola prevalencia HP infekcie u 52 % pacientov s GERD a 62 % v kontrole. Rozdiel v zastúpení CagA u pacientov s GERD bol 44,4 % a v kontrole 87 %. Zastúpenie CagE 44 %, resp. 64 %. CagA aj CagE 25,7 %, resp. 54,8 %.
V skupine pacientov s karcinómom žalúdka (po prísnych exkluzívnych kritériách: bez antisekrečnej liečby, chirurgickej revízie, HP eradikácie) zredukovanej na 160 pacientov s karcinómom žalúdka bolo 110 HP pozitívnych.
Ani v súčasnosti nie je jednoznačne definovaný vplyv infekcie HP a jej liečby na vývoj GERD. Pozoruhodné je najmä odôvodnenie patofyziológie odvodzujúcej riziko exacerbácie GERD na základe miesta postihnutia žalúdka HP infekciou. Vplyv môžu mať typy dispozície cytotoxínového génu kmeňov HP a možný účinok nielen na sekréciu, ale aj na motilitu žalúdka. Rovnako môže mať vplyv dĺžka trvania infekcie HP, čo dokazujú pediatrické štúdie u mladých pacientov, kde zrejme nedošlo k vzniku korporálnej atrofie. Ak by sa pri gastroskopii štandardne bioptovala časť antra aj tela žalúdka, mohla by sa liečba preventívne predĺžiť pri zachytení korporálnej HP infekcie/atrofie. Prínosné by mohlo byť štandardné vyšetrenie cytotoxínových asociovaných génov HP, čo je však pre laboratórnu nedostupnosť a finančnú náročnosť v klinickej praxi neaplikovateľné. V každom prípade, strach z navodenia exacerbácie GERD, Barrettovho pažeráka a adenokarcinómu pažeráka nemôže byť dôvodom ustúpenia od eradikačnej liečby, ktorá je indikovaná v prípade nálezu histologicky verifikovanej gastritídy, dyspepsie a podľa ostatných indikačných kritérií. Nikdy nebol nepriestrelne preukázaný fakt, že samotná eradikácia HP spôsobí de novo GERD. Prikláňame sa k názoru, že nebyť prítomnej korporálnej atrofie, GERD by sa prejavil už dávno a v týchto prípadoch je sanácia korporálnej HP gastritídy samostatným a významným rizikom k jeho rozvoju. V takom prípade je vhodné pacienta pred eradikáciou poučiť o možnom rozvoji refluxu po úspešnej eradikácii infekcie HP. Viac odborných štúdií sa prikláňa k ústupu duodenogastrického refluxu v prípade úspešnej HP eradikácie.
Zdroj: MUDr. Peter Hyrdel, PhD., Gastroenterológia pre prax 3/2021

To, že naše zdravie je vo veľkej miere ovplyvnené našou stravou, je fakt, ktorý by sme si mali denno denne pripomínať. Faktom je ale aj to, že na to veľmi rýchlo zabúdame vo víre povinností a často aj vo víre náhleho hladu.
Hoci mnohí sú názoru, že raňajky sú základom dňa, dnes už vieme, že je to skôr individuálne. Niekto začína deň bohatými alebo naopak, malými raňajkami, ale niekto až obedom. Každý si nájde to „svoje“ a ono sa to aj často mení. Raz si človek dáva raňajky a inokedy nemá túto potrebu.
Nech je to tak, či onak, mali by sme dbať o vyváženú stravu na makroživinovej, ale aj mikroživinovej úrovni. Nestačí si sledovať príjem bielkovín, sacharidov a tukov, ale dbajme aj o príjem vitamínov, minerálov, ktoré sa v nich skrývajú. Preto je dôležitý zdroj príjmu – ani nie energie – ale živín. Niekedy stačí malá zmena pohľadu napríklad na orechy. Nie sú to len tuky, ale je to aj zdroj esenciálnych živín, ktoré sú nevyhnutné pre správne fungovanie hormónov, mozgu a vyživovanie tela na úrovni stopových prvkov.
Dnes si doprajeme na raňajky pšenovú kašu, ktorá je vhodná aj pre hladošov, pretože z daného – zdanlivo malého množstva surovín vyčarujeme pol kila chutnej a zdravej kaše.
Spravte si takúto kašu večer a nechajte do rána odstáť, kľudne aj na kuchynskej linke. Pri odchode do práce iba schmatneme a ničím sa nezdržiavame. Dobrú chuť.